


第一作者:Tiantian Wang
通讯作者:汪洋
通讯单位:天津大学
论文链接:https://pubs.acs.org/doi/10.1021/acs.est.5c05232
▍成果简介
天津大学的汪洋老师在Environmental Science & Technology期刊发表了名为“Closed-loop Lithium Recovery from Ternary Lithium-Ion Batteries: Dual Utilization of Waste Materials”的论文。本研究以废旧正极材料(SNCMs)为电极,开发了一种“SLNCM//SNCM”摇椅式电容去离子(RCDI)系统,用于从废电池浸出液中高效优先回收锂。该系统每循环可实现4.90 mmol g⁻¹的连续选择性锂提取,接收液中Li⁺纯度高达95.82%,整个提取过程的锂回收率约为90.9%。基于“SLNCM//SNCM”RCDI系统,本研究还设计了一种闭环回收策略,通过将SNCMs同时用作电极和浸出液的双重利用,实现了废料的“自循环”。该系统能耗更低、效率更高且循环稳定性更优,经济分析显示其具有正向收益,凸显了该工艺的可行性和可持续性。这种环保技术符合循环经济和可持续发展原则,为废旧电池回收和资源再利用提供了高效解决方案。
近年来,电化学方法在离子分离领域得到了广泛应用。CDI技术能够选择性回收特定离子,被认为是一种在脱盐、营养物去除和资源回收方面极具前景的方法。该技术流程简单,可通过电极材料和界面工程进行优化,减少二次废物产生,降低环境污染,并保证较高的能源效率。目前,电化学提锂的主要问题在于正负极材料的选择。Li(NiₓCoᵧMnz)O₂三元正极材料利用镍、钴、锰的协同效应,兼具LiMnO₂、LiCoO₂和LiNiO₂的优势。NCM(镍:钴: 锰比例为 1:1:1)具有较高的比容量,同时安全性和循环性能也得到增强。Lawagon等人提出将NCM与Ag配对,构建一种新的电化学系统用于从盐湖卤水中回收 Li⁺,从盐水中实现了96.4%的Li⁺纯度。与卤水不同,废旧三元电池浸出液中的阳离子主要包括Li⁺、Ni²⁺、Co²⁺和 Mn²⁺。Ni²⁺(0.7Å)、Co²⁺(0.72Å)和Mn²⁺(0.70Å)的离子半径与Mg²⁺相近,这表明浸出液中的Li⁺更易嵌入NCM晶格中。此外,NCM电池的废旧正极材料(记为SNCM)尽管容量和循环性能有所衰减,但在电化学提锂方面仍具有巨大潜力。
此前,大多数电化学提锂方法采用传统的CDI技术,该技术为间歇式工艺,需要单独的吸附和再生步骤。RCDI作为一种新兴的电化学脱盐技术,无需单独的再生步骤即可实现连续脱盐,且能耗更低、电荷效率更高、循环稳定性更优。Lee等人提出了一种用于连续苦咸水脱盐的RCDI系统,该系统由一对Nafion涂层活性炭电极和一张阴离子交换膜组成,实现了连续脱盐。在此基础上,Yin等人开发了一种“LiFePO₄/FePO₄”RCDI装置,用于从盐湖卤水中提取锂离子,展现出良好的锂富集能力和循环性能。因此,通过采用SNCMs作为电极材料构建“SLNCM/SNCM”RCDI装置,该系统旨在实现低能耗、从三元浸出液中连续优先回收锂,同时实现废料的循环再利用。
本研究采用SNCMs作为电极材料构建了“SLNCM/SNCM”RCDI装置,并全面研究了该系统的电化学行为。通过在模拟浸出液和实际浸出液中对系统进行初步实验,实现了锂的优先选择性回收。此外,通过加入提纯步骤,成功在接收液中回收得到高纯度Li⁺,为后续回收Ni、Co和Mn创造了便利条件。最后,本研究提出了废旧三元锂离子电池的闭环回收策略,并进行了经济分析。同时,将SNCMs同时用作电极材料和浸出液,实现了废料的双重利用。该方法为废旧镍-钴-锰电池材料的环保高效回收提供了新策略,旨在推动循环经济发展。
▍图文导读
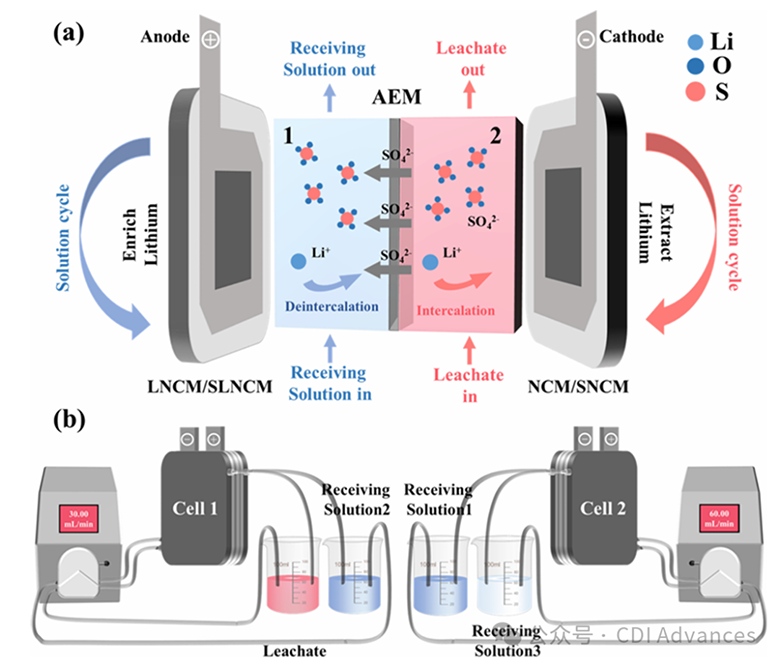
Figure 1. (a) Principle of lithium extraction using the “LNCM//NCM”/“SLNCM//SNCM” rocking-chair CDI system. (b) Over all process of lithium extraction, where Cell1 is used for initial lithium extraction and Cell 2 is for lithium purification.
提锂流程如图1a所示:阴离子交换膜将电池分为两个腔室,分别记为腔室1和腔室2;LNCM和NCM(即SLNCM和SNCM)分别用作阳极和阴极;初始提锂电池记为电池1,锂提纯电池记为电池2;所有接收液的体积均为50 mL。
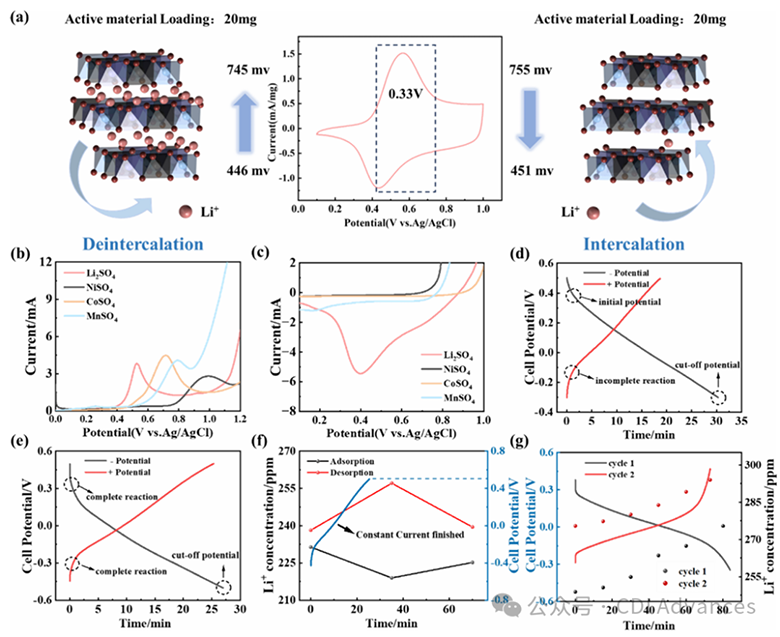
Figure 2. (a) Schematic of Li+deintercalation/intercalation in “LNCM//NCM” rocking-chair CDI and CV of NCM in Li2SO4 Article solution, (b) LSV of LNCM during forward scan in different solutions, (c) LSV of NCM during reverse scan in different solutions; effects of cut off potential during constant potential processes, (d) asymmetric reaction and (e) symmetric reaction; (f) effect of the duration of constant voltage and (g) Li+ deintercalation/intercalation behavior during the single constant potential process.
如图2a所示,阳极和阴极的电势(相对于Ag/AgCl)变化如下:锂离子不断从阳极脱嵌,使阳极电势从446 mV逐渐升至745 mV;相反,锂离子不断嵌入阴极,使阴极电势从755 mV逐渐降至451 mV。这种电势变化表明阳极和阴极的反应是对称的。从电极在Li₂SO₄溶液中的CV结果可以看出,该电势变化范围恰好处于锂的脱嵌与嵌入区间内。此外,LSV验证了锂离子在NCM中嵌入/脱嵌的特异性。图2b中的正向扫描显示,在不同溶液中,仅在各起始电势处出现锂离子脱嵌的氧化峰;图2c中的反向扫描显示,在锂离子嵌入电极的过程中,仅锂离子能在该电势范围内嵌入,出现还原峰,且无其他氧化还原反应发生。为实现摇椅式CDI电池中阳极和阴极的对称反应,需仔细研究其工作电压。LNCM预脱锂后,作为阳极的LNCM与作为阴极的NCM之间的电势差约为0.32 V,且反应结束时两电极间的电势应达到−0.32 V。如图2d所示,当截止电势设为−0.32 V时,下一循环的初始电势值仅为−0.15 V左右。若以将下一循环的初始电势设定在−0.32 V左右为目标(如图2e所示),则需将截止电势设为−0.5 V。这是因为克服离子穿过膜的渗透压以及打破反应的能垒需要额外的能量。
除施加电压外,其施加时长也是一个重要的操作参数,如图2f所示。当恒流达到截止电势时,恒压阶段开始,此时阳极侧的Li⁺浓度从238.17 ppm增至257.07 ppm,而阴极侧的Li⁺浓度从231.38 ppm降至218.98 ppm。随着恒压继续施加35分钟,阳极侧的Li⁺浓度降至239.43 ppm,阴极侧的Li⁺浓度增至225.20 ppm,这可能与锂离子持续的嵌入/脱嵌密切相关,导致电极间的电势差减小,即驱动力减弱。因此,需控制恒压时长,以防止脱嵌和嵌入反应发生部分逆转。为验证上述发现,进一步开展了连续两个循环中仅采用恒流过程的锂脱嵌实验。图2g显示,在电势达到截止电势前,Li⁺浓度持续上升。值得注意的是,由于第一个循环未达到截止电势,第二个循环中Li⁺浓度的增幅(18.55 ppm)小于第一个循环(26.60 ppm)。因此,为保证电池的连续运行,在确保足够恒流的同时,还需设定合理的恒压时间。
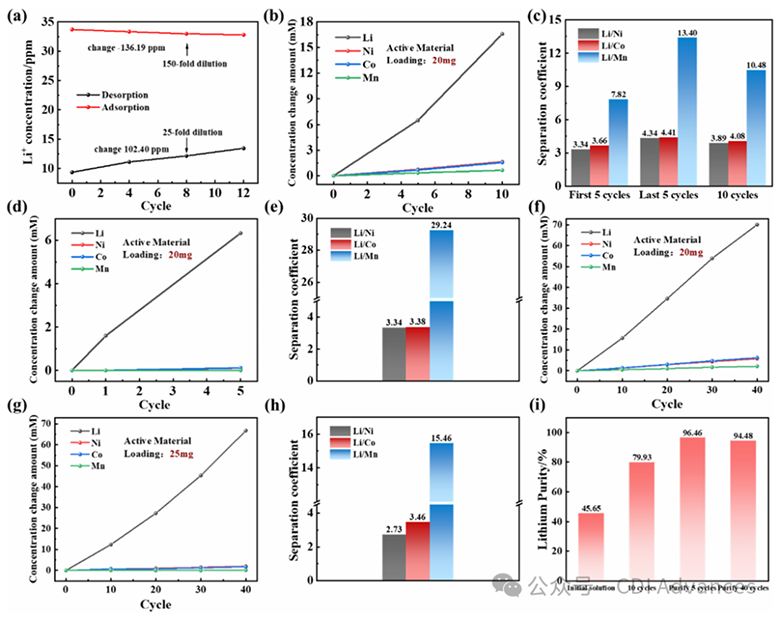
Figure 3. Performance of the “LNCM//NCM RCDI” in simulated leachate: (a) Li+ deintercalation/intercalation in 0.3 M Li2SO4over 12 cycles, (b) initial lithium extraction over 10 cycles, (c) separation coefficients of Li/Ni, Co, Mn, (d) Lithium purification in Cell 2, (e) separation coefficients in 5 lithium purification cycles, (f) initial lithium extraction in Cell 1 for 40 cycles, (g) lithium purification in Cell 2 for 40 cycles, and (h) separation coefficients of Li/Ni, Co, Mn in the whole process; (i) changes in lithium purity during the whole process.
首先在模拟浸出液中测试“LNCM//NCM”摇椅式CDI电池。图3a显示在0.3 M Li₂SO₄溶液中进行12次脱嵌与嵌入循环后,接收液浓度增加约102.40 ppm。此外,如图3b、c及图S3所示,在模拟浸出液中进行初始提锂实验:活性物质负载量为20 mg,循环10次后,接收液中Li⁺浓度增加16.57 mM,Ni²⁺、Co²⁺、Mn²⁺浓度分别增加1.65 mM、1.56 mM、0.65 mM;Li⁺相对于Ni²⁺、Co²⁺、Mn²⁺的分离系数分别为3.89、4.08、10.48;每循环可提取4.96 mmol·g⁻¹的Li⁺(所有容量均按活性物质质量计算),接收液中锂纯度从45.65%提升至81.08%。前5个循环与后5个循环的选择性及吸附量相当,且后者略有提升。在电池1中完成10次初始提锂后,进一步在电池2中验证锂提纯过程(如图3d、e及图S4所示),结果显示接收液中锂纯度达到96.46%,证实了提纯步骤的可行性。此外,对两个串联运行的电池进行了40次长期循环实验,结果如图3f−i所示。经过40次初始提锂循环后,接收液1和接收液2中Li⁺的总浓度增加了70.10 mM,Ni²⁺、Co²⁺和Mn²⁺的浓度分别增加了5.79、6.29和2.20 mM,平均每循环提取5.26 mmol·g⁻¹的Li⁺。再经过40次锂提纯循环后,Li⁺浓度增加了66.71 mM,Ni²⁺、Co²⁺和Mn²⁺的浓度分别增加了2.02、1.73和0.14 mM,平均每循环提取4.00 mmol·g⁻¹的Li⁺。由于稀溶液中动力学较慢,提纯过程中单位电极质量的锂提取量较低。Li⁺相对于Ni²⁺、Co²⁺和Mn²⁺的平均分离系数分别为2.73、3.46和15.46,接收液3的锂纯度达到94.48%。该装置在长期循环中运行稳定,且Li⁺对Ni²⁺、Co²⁺和Mn²⁺的选择性更高,这归因于它们的离子半径不同。
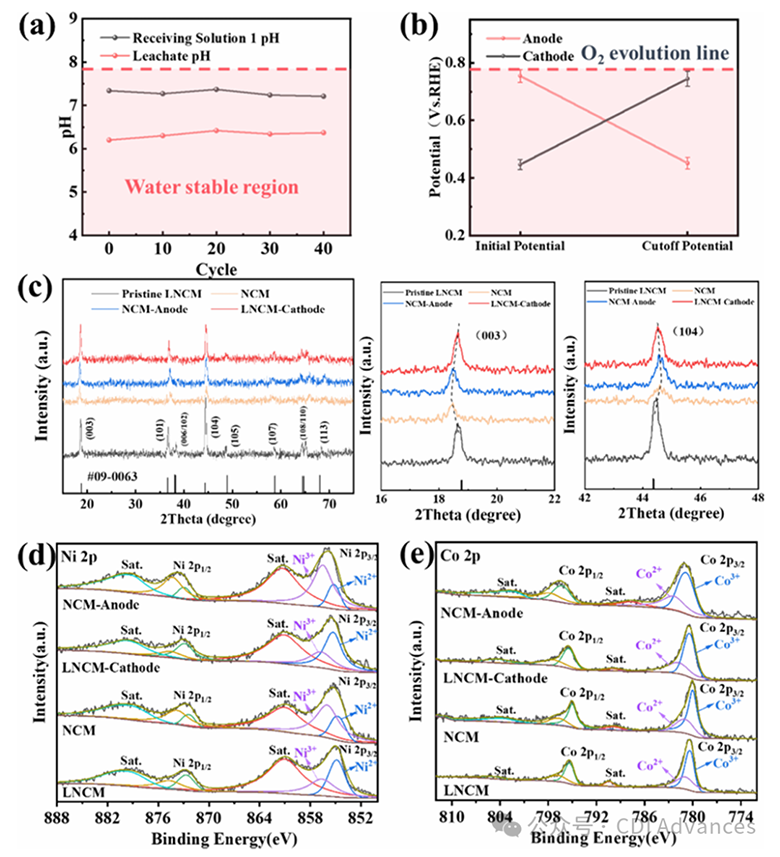
Figure 4. (a) pH changes in the cathode and anode chambers during 40 initial lithium extraction cycles, (b) electrode potential changes during reaction, and (c) XRD patterns and high-resolution XPS spectra. (d) Ni 2p and (e) Co 2p of pristine LNCM, predelithiated NCM, and postcycling cathodes and anodes.
材料稳定性是电化学提锂技术的显著短板,因此也受到了进一步关注。图4a、b监测了电池1中阴极腔室和阳极腔室在40个循环中的pH变化以及每循环的电极电势变化。阴极腔室的pH在6.2~6.42之间波动,阳极腔室的pH在7.22~7.39之间波动。每10个循环的平均阳极电势在0.447±0.018 V~0.745±0.026 V之间波动,阴极电势在0.755±0.023 V~0.451±0.0205 V之间波动。这些变化均发生在H₂和O₂析出线以及水稳定区的范围之外。图4c呈现了在模拟浸出液中循环前后阴极和阳极的XRD图谱。循环后阴极的特征峰与原始LNCM几乎一致,阳极的特征峰也与脱锂后的NCM基本吻合。NCM材料中锂离子的脱嵌与嵌入通过Ni²⁺/Ni³⁺的氧化还原反应实现,而Co和Mn的价态变化极小。图4d、e及图S8中的XPS分析证实,循环后阴极和阳极中Ni²⁺/Ni³⁺的比例与原始LNCM和预脱锂NCM相近,且Co和Mn的价态无明显变化。
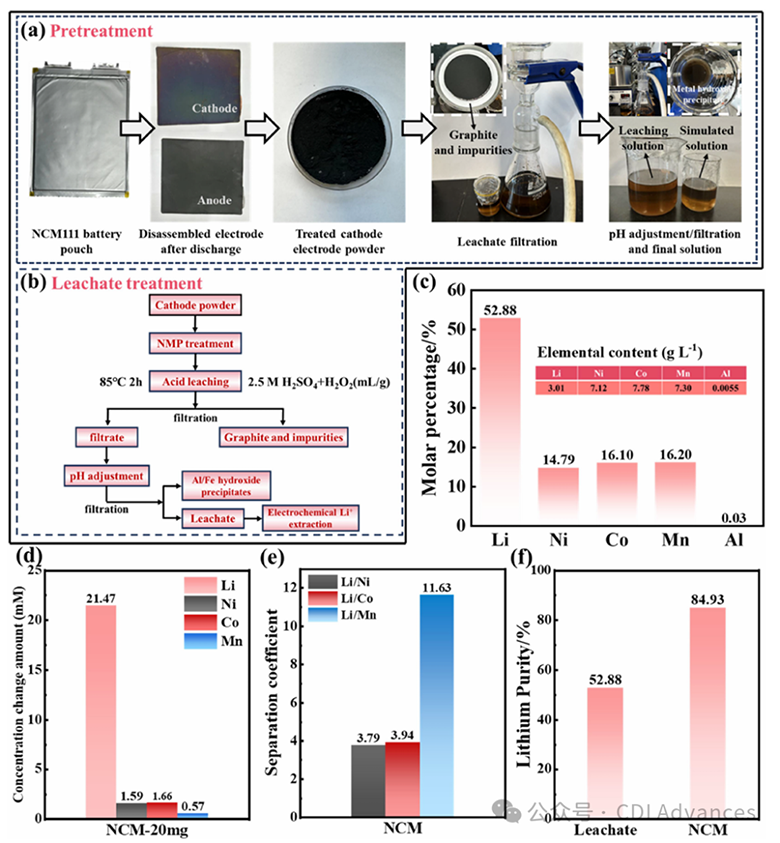
Figure 5. (a) Disassembly and leaching process of spent batteries, (b) flowchart of the leaching process, and (c) composition of the leachate. Performance of the “LNCM//NCM” RCDI system in the leachate: (d) initial lithium extraction over 10 cycles, (e) separation coefficients of Li/Ni, Co, and Mn, and (f) changes in lithium purity during the whole process.
从废旧电池浸出液中提取锂。废旧电池的拆解与浸出具体流程如图5a、b所示。首先对电池进行放电以确保安全,随后在通风橱中使用锯子和钳子手动拆解,分离出正/负极材料。采用NMP溶解PVDF粘结剂,使正极活性材料与铝集流体分离。将正极碎片置于NMP中,在100°C下处理24小时,随后过滤并在140°C真空干燥箱中干燥。干燥后的粉末在空气中于550°C下煅烧,以去除碳和残留有机物,之后将正极在2.5 M H₂SO₄+H₂O₂混合溶液(H₂O₂用量为每克正极材料对应若干毫升)中浸出,浸出条件为:温度85°C,时间2小时,固液比1:10。38浸出液经过滤后,用3 M NaOH调节pH以沉淀残留的铝,随后将pH调至6.2左右。浸出液的组成如图5c所示,其中Li⁺纯度约为52.88%,略高于模拟溶液。在浸出液中进一步验证了“LNCM//NCM”RCDI系统回收锂的可行性。图5d−f显示了在活性物质负载量为20 mg的条件下,10次初始提锂循环的结果:接收液中Li⁺浓度增加了21.47 mM,Ni²⁺、Co²⁺、Mn²⁺浓度分别增加了1.59 mM、1.66 mM、0.57 mM;每循环Li⁺提取量为5.37 mmol·g⁻¹,锂离子纯度从浸出液中的52.88%提升至84.93%。这些结果与之前在模拟浸出液中的提锂结果高度一致,表明“LNCM//NCM”RCDI系统从实际浸出液中回收锂是可行的。
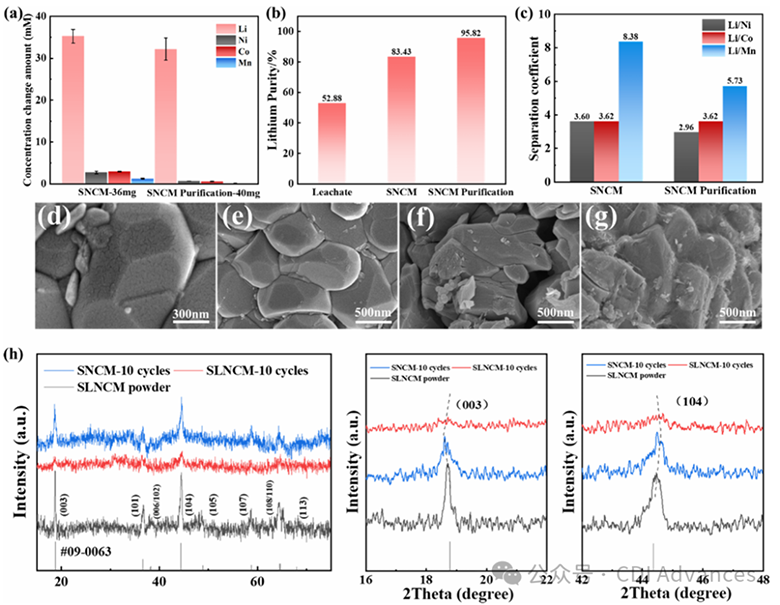
Figure 6. Performance of the “SLNCM//SNCM” rocking-chair CDI in leachate: (a) SNCM electrodes (Cell 1 with 36 mg of active material, Cell 2 with 40 mg of active material ) over 10 initial lithium extraction cycles and 10 lithium purification cycles, (b) changes in lithium purity, (c) separation coefficients of Li/Ni, Co, and Mn, SEM images of (d, e) SNCM powder, (f) ”SLNCM//SNCM” cathode, and (g) “SLNCM//SNCM” anodeafter10 Lithium extraction cycles, and (h) XRD patterns of SNCM powder and the SNCM cathode/anode.
基于这些结果,围绕循环经济和零排放目标,本研究将废旧电池的正极材料(SNCMs)应用于浸出液中的锂回收。如图6a−c所示,SNCM用于10次初始提锂循环及后续的10次锂提纯循环。在初始提锂过程中,接收液中Li⁺浓度增加35.26 mM,Ni²⁺、Co²⁺、Mn²⁺浓度分别增加2.74 mM、2.97 mM、1.29 mM;每循环Li⁺提取量为4.90 mmol·g⁻¹,Li⁺相对于Ni²⁺、Co²⁺、Mn²⁺的分离系数分别为3.60、3.62、8.38。在提纯过程中,接收液中Li⁺浓度增加32.19 mM,Ni²⁺、Co²⁺、Mn²⁺浓度分别增加0.66 mM、0.59 mM、0.16 mM;每循环Li⁺提取量为4.02 mmol·g⁻¹,Li⁺相对于Ni、Co、Mn的分离系数分别为2.96、3.62、5.73。经过这两个步骤后,锂离子纯度先从52.88%提升至83.43%,进而提升至95.82%。
此外,图6h显示,SNCM粉末的XRD图谱中出现了NCM的所有特征峰,但由于晶体结构存在缺陷,部分特征峰发生了偏移(例如(003)峰向低角度偏移),这有助于恢复晶格对称性。所有电极均保留了NCM的特征峰和结晶度,其中阴极的衍射峰与SNCM粉末高度吻合。这些结果表明,在一定时间内,SNCM能够稳定地从浸出液中回收Li⁺,且其结构缺陷可增强反应活性,使得Li⁺的提取速度快于新鲜NCM。因此,将SNCM正极材料用作摇椅式CDI装置的电极,以优先从浸出液中回收锂是可行的。当SNCM电极达到使用寿命后,可将其中的Li⁺最大限度地提取到接收液中,随后通过浸出处理回收Ni、Co和Mn。
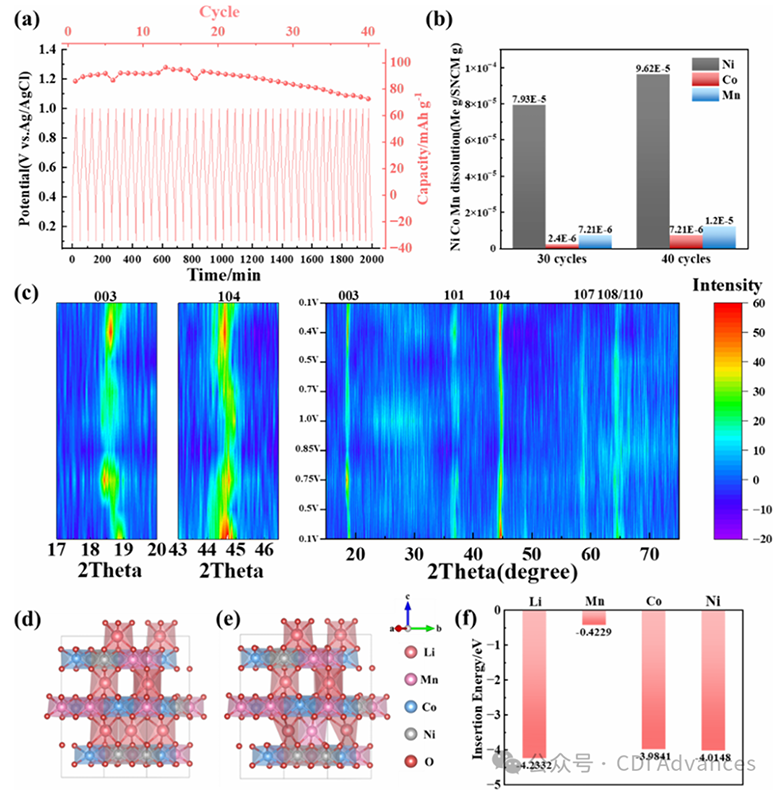
Figure 7. (a) Cycle stability of the SNCM electrode over 40 charge−discharge cycles, (b) dissolution of transition metals from the SNCM electrode, (c) “quasi-in-situ” XRD of the SNCM electrode during Li+ intercalation/deintercalation (d) Li6Mn9Co9Ni9O54−Li model, (e) Li6Mn9Co9Ni9O54Mn model, and (f) intercalation energies of Li+, Ni2+ , Co2+; and Mn2+ into Li6Mn9Co9Ni9O54.
经过40次循环后,SNCM的放电容量从峰值96.56 mAh·g⁻¹降至72.74 mAh·g⁻¹,容量保持率为75.33%。图7b显示了30次和40次循环后SNCM中过渡金属的溶解情况,其中镍的损失率在过渡金属中最为显著,但仍低于0.01%。此外,通过图7c中SNCM的“准原位”XRD图谱可探究其在Li⁺脱嵌/嵌入过程中的结构变化。从下到上,图谱分别对应充电过程中不同电势(相对于Ag/AgCl):0.1、0.5、0.75、0.85和1 V,以及放电过程中的0.7、0.5、0.4和0.1 V。充电时Li⁺脱嵌,(003)峰向低角度偏移,(104)峰向高角度偏移;在0.5 V时,Li⁺开始从SNCM中明确脱嵌,当电势处于0.75~0.85 V之间时,(003)和(104)峰停止偏移,表明Li⁺脱嵌可忽略不计。放电时Li⁺嵌入,(003)和(104)峰向与脱嵌相反的方向偏移;在0.7 V时,Li⁺开始嵌入SNCM,当电势处于0.4~0.1 V之间时,Li⁺嵌入停止,峰位恢复至初始状态,由此可见SNCM中Li⁺的脱嵌与嵌入具有可逆性。
采用具有约75%锂空位的Li₆Mn₉Co₉Ni₉O₅₄模型进行密度泛函理论(DFT)计算(图7d−f及图S18)。结果显示,在还原反应中,Li⁺的吉布斯自由能变(ΔG)最负,其次是Ni²⁺、Co²⁺,而Mn²⁺的ΔG负性最弱。这表明Li⁺的结合能力最强,且Li⁺与Mn²⁺之间的选择性差异最显著,这与提锂结果一致。此外,Ni²⁺、Co²⁺、Mn²⁺的水合能分别为−2121、−2046和−1840 kJ·mol⁻¹,而Li⁺的水合能为−515 kJ·mol⁻¹。Li⁺的绝对水合能最小,使其在电场作用下更容易失去水合壳层,率先到达电极表面。相比之下,Ni²⁺、Co²⁺、Mn²⁺必须克服较高的脱水能垒,导致动力学较慢。这也是NCM对Li⁺具有选择性的一个关键因素。
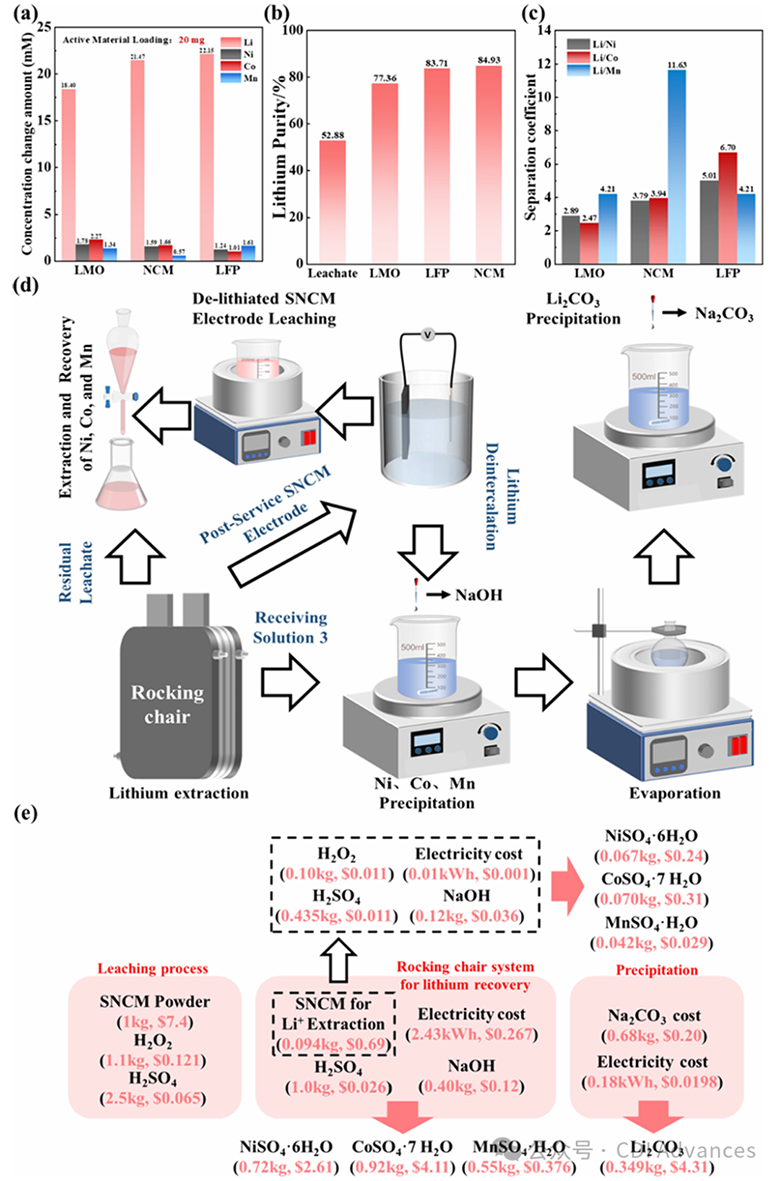
Figure 8. Comparison of lithium extraction performance for LMO, LFP, and NCM in leachate over 10 cycles: (a) lithium extraction capacity, (b) separation coefficients of Li/Ni, Co, Mn, and (c) lithium purity, (d) closed-loop recycling strategy for the “SLNCM//SNCM” rocking-chair CDI, and (e) economic analysis for the recycling process.
锂选择性材料对比及经济性分析。进一步制备了NCM、LMO和LFP(活性物质负载量均为20 mg),并在摇椅式CDI电池中对比其Li⁺提取性能(图8a−c)。LMO、LFP和NCM的Li⁺提取量分别为18.40、22.15和21.47 mM,对应每循环每单位电极质量的提取量分别为4.60、5.53和5.37 mmol·g⁻¹;10次循环后,提取的Li⁺纯度:LMO为77.36%,LFP为83.71%,NCM为84.93%。综合Li⁺提取量和纯度来看,LFP的性能与NCM相当,而LMO较差。此外,NCM对Li⁺/Mn²⁺的选择性显著,LFP则在Li⁺/Ni²⁺、Li⁺/Co²⁺和Li⁺/Mn²⁺之间表现出更均衡的选择性,但由于LFP中存在一维锂离子通道,其提锂过程的动力学较慢,且NCM的电导率约为10⁻⁶ S·cm⁻¹,显著高于LFP(约10⁻⁹ S·cm⁻¹),因此与NCM相比,LFP提锂需要更长的反应时间和更高的能耗。综上,采用上述“SLNCM//SNCM”RCDI系统可实现锂的回收,完成提锂循环后,对废弃的SNCM电极进行电化学脱锂和浸出处理,可构建废旧三元锂离子电池的闭环回收流程,该方法不仅能规避NCM的高成本,还能促进废弃电极材料的回收再利用,符合循环经济和零排放理念。
最后,图8d、e估算了利用SNCM从三元材料浸出液中回收锂的经济效益。以回收1 kg SNCM粉末为例,该流程设定为80个循环,初始提锂和锂提纯电池中共有94 g SNCM电极,以及7 L浓度为5 mM的Li₂SO₄接收液。向接收液中加入NaOH以去除杂质(Ni、Co、Mn),随后蒸发浓缩至Li⁺浓度>20 g·L⁻¹。通过加入Na₂CO₃沉淀得到Li₂CO₃,最终经过滤和干燥处理。SNCM电极中残留的锂通过电化学脱锂转移至接收液中去除,之后对电极进行浸出并通过溶剂萃取处理。提锂后,采用溶剂萃取分离残留的浸出液。该流程的锂回收率为78%,Ni、Co、Mn的回收率为80%。主要成本包括SNCM粉末(1.094 kg,8.09美元)、H₂O₂(1.2 kg,0.132美元)、H₂SO₄(3.935 kg,0.102美元)、Li₂SO₄(0.011 kg,0.105美元)、NaOH(0.52 kg,0.156美元)、Na₂CO₃(0.68 kg,0.20美元)以及电力(2.62 kWh,0.288美元)。产出包括Li₂CO₃(0.349 kg,4.31美元)、NiSO₄·6H₂O(0.787 kg,2.85美元)、CoSO₄·7H₂O(0.99 kg,4.42美元)和MnSO₄·H₂O(0.592 kg,0.405美元)。总利润为2.91美元,确保了回收流程的可持续性。
文章来源:CDI Advances
特别声明:本站所载图文内容均来源互联网,微信公众号等公开渠道,我们对文中观点保持中立,出于更直观传递信息之目的转载稿件,仅供参考。版权归原作者和机构所有,并不代表本网赞同其观点和对其真实性负责。如有侵权,或涉及任何第三方合法权利,请及时联系我们删除(微信:snan2109;QQ:906945059),我们会及时反馈并处理完毕。